
Pomanox® e Mediteanox®, estratti mediterranei per la salute cardiovascolare
C.F.M. Co. Farmaceutica Milanese annuncia una nuova importante collaborazione con l’azienda spagnola Euromed, una realtà industriale consolidata e produttore leader nel settore degli estratti botanici.
Euromed è stata fondata nel 1971 dalla casa farmaceutica Madaus; da allora Euromed si è dedicata all’estrazione di sostanze bioattive naturali, innanzitutto per l’industria farmaceutica e poi anche per i settori nutraceutico e cosmetico, mettendo sempre al centro della propria attività la qualità, il rigore e il supporto scientifico e diventando leader mondiale nella produzione di molti attivi di origine botanica tra cui la silimarina dal cardo mariano e l’estratto di Serenoa repens. Oggi Euromed lavora più di 5000 tonnellate di biomassa all’anno in due siti, quello storico di Barcellona e un nuovo stabilimento ad elevata automatizzazione nell’area di Murcia.
Proprio presso il sito di Murcia, all’avanguardia per le tecnologie utilizzate, vengono prodotti Pomanox® e Mediteanox® due tra le referenze di una linea di estratti di notevole interesse per il settore degli integratori alimentari. Pomanox® e Mediteanox® sono estratti con sola acqua mediante una tecnologia brevettata ed eco-friendly denominata Pure-Hydro™ Process, che impiega acqua osmotizzata.
Pomanox® è un estratto di melograno ottenuto da frutti freschi provenienti da coltivazioni rigorosamente spagnole e sotto il controllo di Euromed. L’estratto è standardizzato in Punicalagine (Alfa e Beta), biomolecole solubili della famiglia degli ellagitannini e caratterizzate da un elevato potenziale antiossidante, mentre l’uso di sola acqua come solvente evita l’estrazione di alcaloidi e altre molecole non sicure per la salute. La standardizzazione è al 15%, 20% o 30% punicalagine, mentre nel processo estrattivo l’acido ellagico viene volontariamente contenuto ad un valore massimo dell’8%: per quanto si tratti del naturale prodotto di idrolisi delle punicalagine (ad esempio da parte del microbiota intestinale), l’acido ellagico è poco solubile e scarsamente biodisponibile ed un suo eccesso riduce l’effettivo potenziale salutistico dell’estratto. Mediteanox® è invece estratto, sempre attraverso il processo Pure-Hydro™, dal frutto delle olive, standardizzato fino ad un massimo di 40% idrossitirosolo, il noto composto fenolico dall’elevato potere antiossidante, in particolare verso le LDL plasmatiche. La combinazione dei due ingredienti può offrire stimolanti prospettive per la realizzazione di integratori “multifunzionali” nell’area cardiovascolare: Pomanox® infatti agisce più selettivamente nei confronti delle problematiche ipertensive e della salute endoteliale mentre Mediteanox® protegge le lipoproteine plasmatiche dall’ossidazione, che è uno dei trigger del processo aterosclerotico.
Insieme. Pomanox® e Mediteanox® supportano quindi il sistema cardiocircolatorio in modo complementare, e diversi studi scientifici, in modelli animali e nell’uomo, hanno investigato questi aspetti sia individualmente sia per la combinazione dei due ingredienti. Pomanox®, Mediteanox® e gli altri ingredienti del catalogo Euromed sono disponibili da C.F.M. Co. Farmaceutica Milanese SpA.
Pomanox® e Mediteanox®: benefici cardiovascolari individuali e combinati
Pomanox® è un estratto di melograno standardizzato in punicalagine, polifenoli della classe degli ellagitannini che si sono dimostrati avere un potere antiossidante rilevante e responsabili di circa metà del potenziale salutistico di questo botanical.
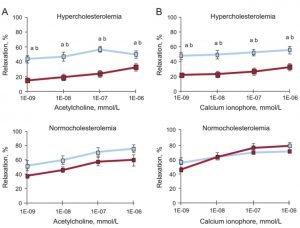
In un interessante studio in modello animale (Vilahur et al., 2015) gli effetti di Pomanox® sono stati valutati somministrando l’estratto (200 mg/die di Punicalagine) a maiali sottoposti ad una dieta normale (NC) o ipercolesterolemica (HC) e misurando la reattività vascolare (ecodoppler) e i marker endoteliali e dell’ossidazione. Gli animali iperlipidemici hanno sviluppato una marcata disfunzione endoteliale osservata come mancato rilassamento vascolare (-50% rispetto agli animali normali) indotto dalla stimolazione con acetilcolina (mediata da recettore) o calcio (mediata da canali ionofori); il trattamento con Pomanox® ha ripristinato l’elasticità vascolare negli animali con dieta ipercolesterolemica: i valori di elasticità sono infatti risultati significativamente diversi dagli animali con dieta ad alto colesterolo non trattati (P<0.05) mentre si sono rivelati statisticamente non distinguibili dagli animali normolipidemici (p=0.87). Attraverso lo studio dell’espressione proteica si è riscontrato che la dieta HC ha ridotto significativamente l’attivazio ne dell’asse Akt/eNOS (sintesi di Ossido Nitrico, mediatore della dilatazione vascolare); il trattamento con Pomanox® ha invece quasi del tutto ripristinato la normale elasticità vascolare attraverso un significativo incremento della via biosintetica della produzione del NO. Anche lo stato di stress ossidativo è risultato migliorato sia in termini locali, con una riduzione, in seguito al trattamento, della positività al test della 8-OHdG (marker del danno del DNA) delle cellule epiteliali, sia a livello sistemico, con un aumento della resistenza all’ossidazione ex-vivo delle LDL circolanti rispetto agli animali non trattati.
Lo stesso meccanismo d’azione rilevato nello studio descritto è quello ipotizzato dagli autori di un altro studio clinico recente (Torregrosa-Garcia et al., 2019) per spiegare gli effetti positivi ottenuti con la somministrazione di Pomanox®, in questo caso a 26 ciclisti amatoriali; lo studio (controllato, randomizzato e crossover) prevedeva l’assunzione di Pomanox® (225 mg/die punicalagine) o placebo per 15 giorni e poi lo scambio di trattamento tra i due rami. Alcuni parametri della performance sono stati misurati prima e dopo il trattamento sottoponendo gli atleti ad una dura sessione che prevedeva un esercizio ad onda quadra al 70% del massimale, un test incrementale fino al massimale e poi prove di esercizio eccentrico e prove di forza. Pomanox® ha incrementato significativamente il tempo totale per giungere all’esaurimento delle forze (TTE, Time to Exhaustion) e il tempo per raggiungere la soglia ventilatoria 2 (VT2, soglia anaerobica o del lattato); si tratta quindi di evidenze che indicano che l’estratto di melograno ha migliorato sia la performance massimale che quella submassimale e la promozione della vasodilatazione (e quindi la facilitazione del flusso sanguigno in corrispondenza dei muscoli) attraverso l’incremento di Ossido Nitrico è una delle possibili spiegazioni di questi effetti. Gli effetti della somministrazione di idrossitirosolo (molecola in cui è standardizzato Mediteanox®) a beneficio del sistema cardiovascolare sono stati variamente dimostrati; anche EFSA ha riconosciuto tali effetti, in particolare per la riduzione della perossidazione del colesterolo LDL, e ha quindi autorizzato un claim specifico. Per quanto concerne Pomanox®, oltre agli effetti già descritti sulla salute endoteliale e sullo stress ossidativo, in diversi studi si è osservato anche un interessante trend di impatto positivo nei confronti della pressione sanguigna.
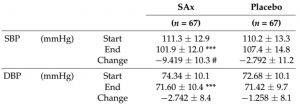
In uno studio RCT crossover recentemente pubblicato (Quiros-Fernandes et al., 2019), Pomanox® e Mediteanox® sono stati quindi combinati in un unico integratore contenente 10 mg di idrossitirosolo e 195 mg di punicalagine per dose giornaliera; il prodotto è stato somministrato contro placebo ad un totale di 67 soggetti di mezza età e apparentemente sani, divisi in due gruppi, per 8 settimane prima di un mese di wash-out e del successivo scambio di trattamento. Se ne è valutato quindi l’effetto su una serie di parametri quali la pressione sistolica e diastolica e la dilatazione flusso-mediata (FMD) dell’arteria brachiale, considerata un indicatore della funzione endoteliale e possibile predittore di eventi cardiovascolari. Nei soggetti trattati si è osservata una riduzione significativa della pressione sistolica (-9.42 mmHg, corrispondente a – 8.5%, p<0.001), significativamente superiore anche alla variazione del ramo del placebo (-2.79 mmHg). Anche la pressione diastolica ha subito una riduzione significativa nei soggetti trattati tra inizio e fine trattamento: -2.74 mmHg, ovvero –3.7%, p<0.05 contro un placebo che non ha visto una riduzione sensibile. La dilatazione flusso-mediata dell’arteria brachiale (FMD) è misurata con tecnologia ecodoppler come aumento % di dilatazione del vaso sanguigno tra momento t0 e un momento finale 70’’ dopo una momentanea interruzione del flusso sanguigno con un bracciale gonfiabile; un valore % maggiore è indice di maggiore elasticità e di una minore disfunzione endoteliale.
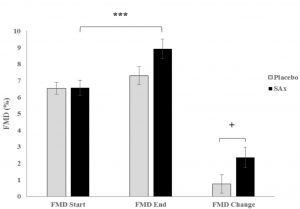
Il trattamento con Pomanox® e Mediteanox® ha provocato un aumento significativo della FMD da 8.04% a 9.46% (p<0.05) mentre i soggetti trattati con placebo non hanno avuto variazioni apprezzabili. Si è anche osservato che selezionando specificamente i soggetti con disfunzione endoteliale (risultati essere quasi il 70%, anche se clinicamente sani), essi hanno avuto, rispetto all’intero campione, incrementi anche più marcati e particolarmente significativi dopo il trattamento con l’integratore, da 6.57% a 8.93% (+2.36 p<0.001), mentre il placebo non ha fornito risultati valutati significativi (figura sotto). Anche la misurazione delle LDL ossidate ha rivelato una loro riduzione significativa nei soggetti trattati e un effetto trascurabile nel ramo del placebo. Lo studio ha quindi permesso di osservare che l’assunzione di idrossitirosolo e punicalagine ha un effetto protettivo verso il sistema cardiovascolare attraverso un miglioramento dell’elasticità vascolare, della pressione sanguigna e dello stato ossidativo.

Coenzima Q, statine e salute cardiovascolare
Le statine sono uno dei farmaci più diffusi, in particolare nei paesi occidentali e rappresentano uno dei trattamenti più efficaci per il controllo delle dislipidemie e quindi per la riduzione del rischio cardiovascolare e della mortalità ad esse legata.
A fronte di un significativo miglioramento del profilo lipidico ematico (riduzione del colesterolo LDL), tra gli effetti collaterali più comuni legati al consumo delle statine sono annoverabili le miopatie o più in generale i cosiddetti SAMS, Sintomi Muscolari Associati con le Statine che possono manifestarsi a livelli crescenti di gravità.
L’insorgenza di questi effetti collaterali è una causa frequente di interruzione del trattamento farmacologico ma ad oggi non sono state ancora del tutto chiarite le ragioni meccanicistiche per cui essi si manifestano.
Come noto le statine agiscono da inibitori della via biosintetica del colesterolo, antagonizzando l’enzima HMG-CoA reduttasi e impedendo quindi la conversione del HMG-CoA in acido mevalonico. Vi sono varie indicazioni che l’inibizione di questo pathway impatti negativamente anche sulla biosintesi endogena di altre importanti molecole prenilate che condividono la stessa via, tra cui il Coenzima Q10 (ubichinone).
Quest’ultimo è un cofattore ubiquitario nell’organismo con un ruolo fondamentale nel metabolismo energetico mitocondriale e come scavenger radicalico.
L’ubichinolo è la versione innovativa del Coenzima Q10 e notevolmente più biodisponibile; è prodotto esclusivamente da Kaneka ed è disponibile per il mercato degli integratori come materia prima in polvere o in capsule già formulate. Il dosaggio massimo ammesso in Italia è di 200 mg/die, come per il CoQ10 tradizionale, ma garantisce un assorbimento notevolmente superiore nell’organismo e un potenziale antiossidante subito pronto senza necessità di interconversione fisiologica.
Nuove meta-analisi sulla relazione tra Coenzima Q10, statine e mialgie
In merito all’interazione tra trattamento con statine, sintomi mialgici e Coenzima Q, le correlazioni tra
- somministrazione di CoQ10 ed entità dei sintomi muscolari da statine
- assunzione di statine e livelli di CoQ10 circolante
sono state variamente valutate in molti studi clinici, con risultati talvolta eterogenei o poco chiari.
Due meta-analisi di recente pubblicazione si sono poste l’obiettivo di riepilogare e rianalizzare i dati clinici più recenti disponibili su entrambi gli aspetti.
Nella prima meta-analisi, pubblicata sul Journal of American Heart Association (1), che puntava a verificare la correlazione tra somministrazione di Coenzima Q10 e lo smorzamento dei sintomi muscolari, 12 pubblicazioni sono state valutate adeguate a partire dagli 868 studi individuati, scremati attraverso una selezione secondo diversi criteri predefiniti (studi di qualità, in formato RCT doppio cieco, con soggetti sotto trattamento con statine+CoQ10 o statine+placebo); tra queste 12, 9 sono state utilizzate per estrapolare i dati sul dolore muscolare (numero totale di soggetti trattati = 433, di cui 222 nel gruppo CoQ10 e 211 con placebo). Confrontata con il placebo, la somministrazione di CoQ10 ha dimostrato (vedi figura qui sopra) di aver ridotto il dolore muscolare (P<0.001), la debolezza (P=0.006), i crampi (P<0.001) e la spossatezza (P<0.001). La solidità dell’analisi è stata verificata mediante calcoli di randomizzazione e l’eterogeneità del risultato del dolore muscolare è stata confermata nel non avere trovato correlazione significativa né con la dose (100-600 mg/die), né con la durata del trattamento (1-3 mesi), né con la data di pubblicazione.
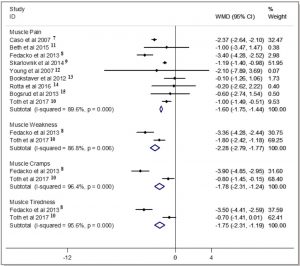
Nella seconda meta-analisi pubblicata sull’European Journal of Medical Research (2), un simile approccio di ricerca di dati e di verifica statistica puntava a verificare la relazione tra assunzione di statine e il livello di CoQ10 circolante. A partire allo screening bibliografico sono risultati adeguati 9 studi clinici RCT doppio cieco, che arruolavano un totale di 1652 soggetti (822 trattati con statine e 830 con placebo).
L’analisi complessiva del campione di individui ha verificato che in effetti il trattamento con statine riduceva significativamente il pool di CoQ10 circolante (p=0.001); l’analisi per sottogruppi condotta negli studi che avevano previsto la distinzione tra tipi di statine ha mostrato che la riduzione del CoQ10 circolante risultava indipendente dal tipo di statina utilizzate (lipofila o idrofila). La variazione non appariva neppure dipendente dall’uso di statine a basso-media o alta intensità né mostrava di essere correlata con la durata del trattamento farmacologico (p=0.994).
Bibliografia
1) Qu et al., J Am Heart Assoc. 2018 Oct 2;7(19)
2) Qu et. al., Eur J Med Res. 2018 Nov 10;23(1):57

InSea2® – Dalle alghe brune un estratto polifenolico per il controllo della glicemia post-prandiale
InSea2® è un ingrediente naturale destinato agli integratori alimentari, sviluppato dall’azienda canadese InnoVactiv e rivolto all’ambito salutistico del controllo della glicemia e della sindrome metabolica.
InSea2 è un estratto secco polifenolico ottenuto mediante estrazione acquosa e successive filtrazioni a partire dalle alghe brune Fucus vesiculosus e Ascophyllum nodosum, che crescono selvatiche nell’oceano Atlantico di fronte alle coste canadesi del Quebec.
Il processo produttivo conduce ad un prodotto con un’elevata concentrazione di polifenoli caratteristici (>20%), principalmente florotannini, ma con un contenuto relativamente ridotto di iodio (<300 ppm), per non influire negativamente sulla funzionalità tiroidea.
I florotannini algali svolgono un’attività specifica e peculiare: assunti insieme al pasto agiscono da blocker reversibili degli enzimi deputati alla digestione intestinale dell’amido e degli oligosaccaridi della dieta (α-amilasi e α-glucosidasi), inibendo in modo dolce ma significativo la scomposizione degli zuccheri complessi assunti con la dieta nelle unità base che li compongono (sostanzialmente glucosio). Ciò determina un effetto analogo a quando si assumono carboidrati a ridotto indice glicemico, ovvero una riduzione nel tempo della disponibilità di glucosio assorbibile e quindi uno smorzamento del picco glicemico post-prandiale con un aumento della coda di assorbimento; tale fenomeno corrisponde ad una diminuzione del picco di insulina richiesto per ricondurre la glicemia ai livelli basali.
L’insulina è l’ormone deputato alla regolazione della concentrazione del glucosio ematico; quando il glucosio entra nel circolo sanguigno l’insulina viene secreta dal pancreas, entra a propria volta in circolo e induce l’esposizione dei trasportatori del glucosio sulle membrane di molte cellule dell’organismo (principalmente epatiche e muscolari) e quindi l’uptake del glucosio.
Il meccanismo è tuttavia naturalmente fragile e suscettibile di essere compromesso. Picchi quotidiani ed elevati di insulina, causati dall’assunzione continua ed abbondante di carboidrati (in particolare quelli ad elevato indice glicemico) provocano una graduale desensitizzazione insulinica che implica che sarà richiesto un apporto sempre crescente di ormone a parità di glucosio da rimuovere dal sangue.
Questo fenomeno induce un progressivo aumento della glicemia a digiuno (un fattore di rischio indipendente di primaria importanza in ambito cardiovascolare) e un circolo vizioso che dall’insulino-resistenza può condurre al Diabete Mellito di tipo 2 a diversi stadi di gravità e a tutti gli stati ad esso connessi, come la Sindrome Metabolica; l’iperglicemia e l’iperinsulinemia sono inoltre stati pro-infiammatori.
Picchi glicemici ed insulinemici post-prandiali molto pronunciati hanno anche ulteriori implicazioni: maggiore è il picco glicemico, più netto è lo stato di temporanea ipoglicemia che segue e che induce cali di attenzione e stati di fame incontrollata, che porta a sovra-alimentazione, aumento di peso ed esacerbazione del circolo vizioso dei carboidrati.
InSea2® assunto al pasto ad un dosaggio di 250mg, smorzando il picco glicemico ad ogni pasto, contribuisce a contrastare i diversi fenomeni descritti, supportando il miglioramento dei parametri glicemici e aiutando a contenere l’incidenza di problematiche di salute connesse con l’insulino-resistenza.
Studi in vitro, in vivo e nell’uomo—efficacia supportata scientificamente
L’efficacia di InSea2® è stata variamente dimostrata in studi in vitro, in modello animale e in studi clinici nell’uomo.
In una recente pubblicazione del 2017 che ha riconfermato risultati già ottenuti in precedenza, i polifenoli algali sono stati impiegati in saggi di inibizione enzimatica in vitro. Gli enzimi α-amilasi e α-glucosidasi incubati in vitro con dosi crescenti di InSea2® sono risultati gradualmente inibiti secondo una dinamica dose/risposta, venendo completamente bloccati con una concentrazione di enzima rispettivamente di 30 e 2 µg/mL (vedi figura).
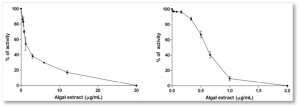
L’attività in vitro misurata in termini di IC50 è risultata superiore a quella dell’acarbosio, un farmaco contro l’iperglicemia e il diabete, con un meccanismo d’azione simile all’InSea2®. In altri studi in vitro si è anche investigata la specificità dell’estratto nei confronti di diverse glicosidasi di mammifero, individuando un’efficacia massima nei confronti della saccarasi di ratto, attività limitata verso la maltasi e nulla nei confronti della lattasi. In un altro studio side-by-side InSea2® ha dato nuovamente prova di avere un’efficacia paragonabile all’acarbosio e significativamente superiore a parità di dosaggio, rispetto ad altri ingredienti naturali (es. faseolamina) con funzione analoga.
Alcuni studi in roditori hanno confermato l’efficacia di InSea2® anche in vivo. In diversi studi condotti nel 2011 in roditori normali, nel 2014 in ratti magri o obesi ed infine nel 2017 in topi modello per la steatoepatite (NASH) non-alcolica umana, InSea2® assunto con un pasto test ha sempre dimostrato di ritardare e/o smorzare il picco glicemico post prandiale e anche il relativo picco insulinemico. In particolare nell’ultimo studio menzionato, l’estratto o un controllo sono stati somministrati ad animali normali o allevati con una dieta ad alto tenore di grassi che dopo 3 settimane ha indotto un significativo aumento di peso rispetto al controllo e l’insorgenza della NASH (steatosi, infiammazione lobulare e fibrosi periportale). In animali normali l’assunzione dell’estratto in concomitanza con un carico glicemico ha ridotto il picco glicemico ed insulinemico a 30 minuti, mentre in animali con steatoepatite (vedi figura sotto) l’effetto dato dal trattamento è risultato notevolmente superiore generando una riduzione significativa sia dei picchi sia dell’area sotto l’intera curva glicemica alle 3 ore.
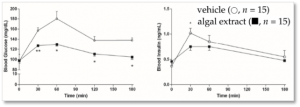
L’efficacia misurata in vitro e i risultati ottenuti in vivo sono stati confermati anche in studi dedicati nell’uomo. Già nel 2011 Paradis e colleghi avevano dimostrato in uno studio crossover che InSea2® (ad un dosaggio di 500 mg) era efficace nella riduzione dell’area sotto la curva (iAUC) del picco glicemico post-prandiale, del relativo picco di insulina e dell’indice Cederholm di sensibilità all’insulina.
Più recentemente, nel 2017, una formulazione di InSea2® e cromo è stata somministrata per 6 mesi a 50 volontari sovrappeso o obesi per valutare il potenziale di miglioramento dei parametri ematici di glucosio ed insulina a digiuno, e non dopo un carico acuto come precedentemente descritto, riducendo quindi il rischio di sindrome metabolica e altre patologie. Dopo il periodo di trattamento sia la glicemia che l’insulinemia a digiuno si sono ridotte in modo significativo (rispettivamente –11% con p<0.001 e – 21% con p<0.05) dopo 6 mesi. Anche l’indice HOMA, un marker accettato di insulino-resistenza, è diminuito nell’arco dei 6 mesi da un valore medio iniziale di 6.1 (ad indicare uno stato di chiara resistenza insulinica) ad un valore significativamente inferiore di 4.4. Inoltre, mentre al t0 nessuno dei soggetti riportava un HOMA inferiore al valore 3, considerato il range di normalità, dopo i 6 mesi di trattamento il 22% dei volontari aveva raggiunto questo valore target, denotando un notevole miglioramento dello stato di insulino-resistenza.
La capacità della stessa formulazione contenente InSea2® di influire positivamente sullo stato glicemico è stata ulteriormente confermata in un ultimo studio controllato con placebo, randomizzato e in doppio cieco di recente pubblicazione (2019).
65 soggetti disglicemici divisi in due gruppi hanno assunto per 6 mesi una formulazione di InSea2 e cromo o un placebo e lo stato glicemico è stato valutato al t0 e al termine del periodo di integrazione misurando diversi parametri (vedi tabella sotto).
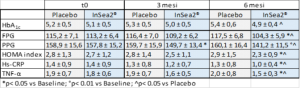
Riduzioni significative sono state rilevate nel gruppo supplementato per i parametri della glicemia basale a digiuno (p<0.05 vs baseline e vs placebo), glicemia post prandiale (p<0.01 vs placebo e p<0.05 vs baseline) e per l’emoglobina glicata HbA1c, un importante indicatore dello stato glicemico permanente dell’organismo (p<0.05 vs placebo). Anche l’indice HOMA relativo all’insulino-resistenza si è ridotto significativamente sia rispetto alla baseline sia rispetto al placebo (p<0.05 per entrambi i casi).
Infine anche la misurazione delle citochine TNF-α e Hs-CRP, rispettivamente marcatore di stati infiammatori e predittore di eventi cardiovascolari acuti, hanno permesso di rilevare riduzioni significative rispetto a baseline e placebo, suggerendo un miglioramento dello stato infiammatorio sistemico.
La cattiva regolazione del glucosio ematico in fase pre-diabetica può esprimersi in termini di IFG (alterata glicemia a digiuno) o IGT (ridotta tolleranza al glucosio). La prima è misurata come livello di glicemia basale superiore alla norma, mentre la seconda si valuta a seguito di un test orale di tolleranza al glucosio (OGTT); entrambe sono condizioni pre-diabetiche e possono condurre al diabete conclamato ma la ridotta tolleranza (IGT) rappresenta un fattore di rischio superiore rispetto alla IFG.
L’evidenza più interessante dello studio è risultata essere che il trattamento con InSea2® e cromo ha indotto una regressione significativa ad uno stato IFG di soggetti che si trovavano in condizione di IGT al t0 e un rientro ad una normale tolleranza al glucosio in soggetti precedentemente in uno stato di alterata glicemia a digiuno IFG (vedi grafico sotto).
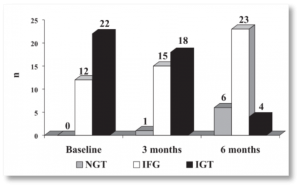

Affron® – Estratto di zafferano di qualità superiore
C.F.M. Co. Farmaceutica Milanese ha recentemente intrapreso una collaborazione con l’azienda spagnola Pharmactive per la distribuzione delle referenze a catalogo. Pharmactive è una realtà dinamica e votata allo sviluppo di ingredienti nutrizionali efficaci e supportati scientificamente e ha il proprio quartier generale a Madrid.
Il prodotto di punta di Pharmactive è Affron®, un estratto di zafferano di qualità superiore.
Affron® è realizzato in completa integrazione verticale, a partire da zafferano coltivato in campi di proprietà nella regione di Castilla-La Mancha. La Spagna è uno tra i Paesi occidentali con i maggiori volumi di produzione di zafferano ma per garantire la titolazione, la qualità e la continuità del prodotto l’integrazione verticale è un requisito indispensabile perché sono necessari tra i 90mila e i 170mila fiori per ottenere 5 kg di stigmi freschi o 1 kg di stigmi secchi, che sono il materiale di partenza per la preparazione dell’estratto, particolarmente delicata. La pianta viene successivamente controllata attraverso tecniche molecolari (genetiche) per accertarne l’identità biologica e viene poi sottoposta ad un processo di estrazione avanzato per proteggere i preziosi attivi contenuti nella droga.
Affron® è standardizzato al 3.5% Lepticrosalidi® mediante metodica HPLC, la più riproducibile e affidabile sotto il profilo analitico; il termine Lepticrosalidi indica il complesso di molecole bioattive contenute nello zafferano, ovvero principalmente la Crocina (somma di diverse isoforme) e il Safranale.
Lo zafferano ed i suoi estratti sono stati tradizionalmente studiati (in particolare in Iran dove questa spezia è particolarmente diffusa) per il loro effetto sull’umore e su blandi stati depressivi.
Le molecole che caratterizzano Affron interagiscono con il Sistema Nervoso Centrale, in particolare con il meccanismo dei neurotrasmettitori; nello specifico risulta che le crocine agiscano come inibitori del reuptake di dopamina e norepinefrina mentre il safranale sul reuptake della serotonina.
Crocine e safranale svolgono anche una funzione antiossidante, anch’essa riconducibile all’ambito del benessere del SNC perché vi sono evidenze che uno sbilanciamento ossidativo e il conseguente danno cellulare possano essere causa di malfunzionamenti a livello neurologico. A supporto di quanto sopra Affron® è l’unico estratto brandizzato e caratterizzato che sia stato valutato ad un dosaggio specifico (28mg) in studi clinici nell’uomo per la sua capacità di influenzare l’umore e modificare blandi stati di ansia e depressione. Si è inoltre osservato un effetto sul miglioramento del sonno.
Affron® è una polvere di un acceso colore arancione, adatta per preparazioni nutraceutiche; è aderente a tutte le normative del settore ed ha una shelf-life di 36 mesi alle condizioni ottimali di stoccaggio.
Studi clinici sull’umore, stati d’ansia e di depressione e sul sonno
In un primo studio RCT pubblicato nel 2017 (Kell et al., Complement Ther Med) Affron è stato valutato per la capacità di migliorare umore, stati d’ansia e di depressione. A tale scopo un totale di 128 partecipanti suddivisi in 3 gruppi hanno ricevuto Affron® a 22 o 28 mg/die oppure un placebo indistinguibile, per un periodo di 4 settimane.
Umore e stato mentale sono stati misurati prima e dopo il trattamento mediante dei questionari di autovalutazione: POMS (Profile of Mood States), PANAS (Positive and Negative Affect Schedule), DASS-21 (Depression Anxiety Stress States).
I soggetti nei diversi gruppi non differivano significativamente alla baseline e si connotavano tutti per uno stato di umore giudicato basso secondo il questionario DASS.
Tra i risultati del questionario POMS si è osservata una relazione significativa trattamento/tempo per i punteggi di tensione, depressione e confusione. Si è inoltre osservato un miglioramento significativo nei punteggi relativi alla fatica e al vigore tra il gruppo con dosaggio di 28 mg/die e il placebo. Complessivamente si è rilevato un miglioramento del punteggio Total Mood Disturbance significativamente più basso per il trattamento a 28 mg/die rispetto al placebo.
Nel questionario PANAS, è stata osservata una riduzione significativa dello stato emozionale negativo per trattamento con Affron® (28 mg) rispetto al placebo.
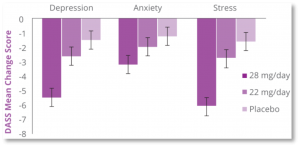
Il questionario DASS-21 ha riportato un effetto significativo nella riduzione del punteggio della Depressione e dello Stress per il dosaggio massimo rispetto al dosaggio intermedio (22 mg) e al placebo; lo stato d’ansia si è invece ridotto significativamente per il dosaggio massimo solo rispetto al placebo. Il bilancio dello studio è stato l’osservazione di un’azione significativa di miglioramento dell’ansia, dell’umore e dello stato di stress da parte di Affron al massimo dosaggio (28 mg/die) rispetto al placebo, senza effetti avversi di rilievo nei volontari trattati, tutti non depressi ma con livelli di umore basso; gli effetti sono stati simili in uomini e donne e hanno replicato risultati precedenti in cui estratti di zafferano avevano prodotto un effetto paragonabile ad alcuni farmaci specifici.
Risultati analoghi si sono ottenuti anche in un altro studio RCT in doppio cieco condotto in questo caso per un periodo di 8 settimane in 68 giovani tra i 12 e i 16 anni, caratterizzati da ansia leggera o moderata e sintomi di tipo depressivo (Lopresti et al., 2018); il trattamento consisteva in 28 mg/die di Affron, contro placebo. I risultati sono stati valutati mediante la compilazione (separatamente sia da parte dei ragazzi sia dei genitori) di un questionario RCADS, Revised Child Anxiety and Depression Scale, giudicato affidabile ed accurato per la rilevazione di stati d’ansia e depressione in bambini e ragazzi. Un’analisi multivariata dei dati ha rivelato una relazione significativa trattamento x tempo. Tra i singoli punteggi, quelli che hanno mostrato variazioni significative nel tempo rispetto al placebo sono risultati: l’ansia da separazione, la fobia sociale, la depressione e l’ansia generalizzata (quasi significativo). Il questionario compilato dai genitori non ha fornito le stesse evidenze ma si tratta di una discrepanza frequente, per via di una differente percezione dei fenomeni psicologici.
Un terzo studio RCT più recente (Nishide et al., 2018, Jpn Pharmacol Ther), è stato condotto nell’ambito della qualità del sonno su un totale di 21 volontari per 4 settimane somministrando Affron, ad una dose contente 0.6 mg/die di crocina, contro placebo. Valutando i soggetti attraverso il questionario PSQI (Pittsburgh Sleep Quality Index) la somministrazione di Affron per 4 settimane ha dimostrato di ridurre significativamente (p=0.04) il punteggio complessivo PSQI. Si è anche osservata una tendenza al miglioramento della disfunzione diurna nel gruppo trattato rispetto al placebo. Tuttavia, suddividendo la popolazione in soggetti con qualità del sonno mediamente buona e scarsa alla baseline, questi ultimi hanno mostrato di beneficare in media in modo marcatamente superiore della somministrazione di Affron sia rispetto al t0 sia rispetto al placebo, al contrario di coloro che già godevano di un buon sonno; ciò si è osservato sia nel punteggio complessivo sia in varie sotto-sezioni del questionario.